Великие открытия
Великие открытия
Деви с новой энергией приступает к исследованиям в области электрохимии. Эта наука непреодолимо влечет его живой ум, здесь — он твердо верит — будут произведены замечательные открытия. Вольтов столб сможет и должен разлагать химические соединения, он явится могущественным средством в поисках новых элементов.
Традиционное ежегодное заседание Королевского общества 20 ноября было посвящено физическим наукам. В 1806 году оно ознаменовалось блестящим докладом Гемфри Деви. Ученый подвел итоги успехам электрохимии и обобщил собственные работы в этой области. Доклад назывался: «О некоторых химических действиях электричества». В нем впервые ставился вопрос о положительном и отрицательном электричестве.
Деви подчеркивал огромное значение электролиза для промышленности, указывал целебные свойства некоторых явлений электричества, предвосхищая развившуюся 125 лет спустя ионную терапию.
«Если рассмотреть электрическую энергию всех тел, то кислород и все тела, содержащие его в большом количестве, окажутся отрицательными, а водород, металлы и все горючие вещества (углеродистые соединения) — положительными».
Каждый факт, добытый в результате эксперимента, способствовал возведению стройного здания теории химического действия электрического тока.
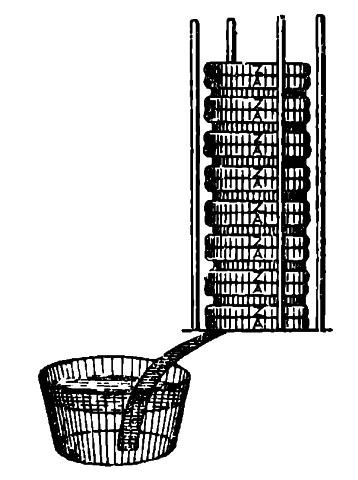
Вольтов столб в его первоначальном виде. Кружки, обозначены буквой А — серебро, и буквой Z — цинк. В нижнем сосуде — разведенная соляная кислота, которая через фитиль смачивала суконные прокладки между каждой парой металлических кружков.
Деви заметил, что если оба полюса Вольтова столба опустить в два сосуда с содой, соединив их полюсы влажным асбестом или бумажным фитилем, то у положительного полюса собирается кислота, у отрицательного — щелочь. Эго подтверждало изменение цвета лакмусовой бумажки. У исследователя тут же возник вопрос, откуда взялись в воде кислота и щелочь?
Рядом остроумнейшим опытов Деви доказал, что щелочь выделяется из стекла сосудов, а соляная кислота — из поваренной соли, всегда существующей в виде примеси в обыкновенной воде. Деви создает теорию, по которой все вещества, обнаруживающие химическое сродство друг к другу, находятся в состоянии противоположного электрического заряда. Поэтому положительный полюс притягивает к себе частицы, заряженные отрицательным электричеством, а отрицательный полюс довершает разрушение, притягивая частицы, заряженные положительным электричеством. Так происходит важнейший процесс — электролиз[15]. Чем мощнее Вольтов столб, тем значительнее сила, разрывающая сложные тела на их составные части. Равновесие рушится, и на свет появляются элементы сложных веществ, до сих пор считавшихся неразложимыми.
Кислота и кислород — тела отрицательные; они притягиваются положительным полюсом, и на нем выделяются металлы и их окиси; водород, азот, углерод положительны — они появляются на отрицательном полюсе.
«В природе непрерывно происходят колебания электрического равновесия. Весьма вероятно, что эти колебания, связанные с явлениями разложения и переноса, существенно изменяют течение химических процессов, разыгрывающихся в различных частях нашей системы.
Электрические феномены, которые предшествуют землетрясениям и вулканическим извержениям, описанные большинством наблюдателей этих событий, можно очень легко объяснить, исходя из вышеустановленной точки зрения.
Наряду с этими внезапными резкими изменениями в различных частях внутренних слоев земного шаря должны происходить изменения электрического состояния, более постоянные и спокойные.
Там, где встречаются слои пирита и слои угольной обманки, где находятся в соприкосновении друг с другом или с каким-нибудь проводником чистые металлы или их сернистые соединения, наконец, там, где различные слои содержат различные соли, должно постоянно обнаруживаться электричество; весьма возможно и то, что действие последнего было существенным для возникновения многих минеральных образований.
Природное электричество до сих пор было мало исследовано, за исключением того случая, когда оно, концентрируясь в атмосфере, делается могущественным и очевидным.
Вероятно, что его медленное и бесшумное действие во всех частях поверхности земли окажется связанным более непосредственным и существенным образом с круговоротом сил в природе; исследования по этому вопросу несомненно прольют свет на науку о земле и, возможно, отдадут в наше распоряжение новые силы».
Деви пришел к твердому убеждению, что можно разложить любое химическое соединение — дело только в силе Вольтова столба.
С кафедры Королевского института на весь мир прозвучали вдохновенные слова Гемфри Деви о том, что может сделать электричество в изменениях и превращениях материи руками человека.
Блестящий доклад Деви подытожил все, что сделало к его времени человечество в области электрических исследований. Слава гениального ученого окончательно утвердилась за Деви.
Иоганн Берцелиус, известный шведский ученый, много позже писал из Стокгольма: «Я проверил и продолжил работы Деви в области электрохимии и подтверждаю, что они являются ценнейшим вкладом в сокровищницу мировой науки».
Чтобы судить о громадном впечатлении, произведенном на ученый мир докладом Деви, достаточно остановиться на одном факте.
После смерти Питта (январь 1806 года) министерство либерала Фокса начало мирные переговоры с Наполеоном, но эти робкие попытки договориться закончились Трафальгаром. 21 октября 1806 года на испанском побережье Атлантического океана, у мыса Трафальгар, произошло морское сражение между английским и французским флотами. В битве погиб национальный герой Англии Нельсон и три тысячи офицеров и матросов английского флота. Флот Наполеона потерял семь тысяч человек. Ценой огромных потерь Англия вторично одержала морскую победу над Францией.
Испанские берега стали свидетелями морской трагедии, закончившейся гибелью многих тысяч людей. Жестокая буря, разыгравшаяся вслед за сражением, докончила то, что не успели сделать пушки военных кораблей.
Борьба между капиталистическими хищниками Европы все более обострялась. Наполеон издает известный приказ о блокаде европейских гаваней. Он объявляет английские товары и английские суда добычей каждого желающего.
В этот напряженный момент французская Академия присуждает Гемфри Деви награду в три тысячи франков за лекцию по электрохимии. Нетрудно представить себе действительное значение работ Деви, если, несмотря на острейшую ненависть правящих клик Франции ко всему английскому, французская Академия все же присудила англичанину Деви почетную премию. Со всех концов земного шара приезжали в Париж ученые для апробации своих открытий и исследований. Целый год занималась французская Академия «проверкой» гениальных работ Алессандро Вольта, а теперь наградила ученого по ту сторону Ламанша!
Как отнеслись к этой награде в Лондоне? Деви принял премию, вызвав ожесточенный вой лондонских газет. Они возмущались антипатриотическим поступком профессора Королевского института, предлагали вернуть деньги парижским «негодяям», грозили расправой. Но все оказалось безрезультатным, — Деви гордился признанием лучшей Академии, наука была для него дороже интересов Даунинг-стрит[16]. Клуб «Тепидариев» мог вполне гордиться своим членом.
Наступил 1807 год, великий год в жизни Гемфри Деви. Деви был избран одним их трех секретарей Королевского общества, Янг и Волластон — двумя другими.
Красной нитью, прошедшей через всю последнюю лекцию Деви, была мысль, что никакое сложное тело, если оно действительно сложное, не сможет противостоять электрическому току достаточной силы. Оно будет разрушено, разложено на свои простые составные части. Из года в год уверенность эта росла; найдено было звено, ухватившись за которое можно будет вытащить на свет дневной цепочку новых, дотоле неизвестных, элементов.
Деви перебирал в своей памяти историю открытия химических элементов. Минувшие столетия проносились перед его умственным взором.
Мышьяк — серовато-белые кристаллы, открытые в XIII веке Альбертом Великим. Далеко из тумана веков вырисовывается силуэт этого замечательного человека. Он не был королем или вельможей, и титул «Великий» получил за необыкновенную эрудицию и глубину научных познаний. Увы, за эти же качества он был обвинен в колдовстве. Деви знал не одну легенду, связанную с этим полумифическим человеком.
Сурьма — XV век — алхимик Василий Валентин. Металлический блеск позволяет отнести сурьму к семье металлов.
Железо, медь, олово, ртуть — известны со времен глубокой древности. Пять тысяч лет прошло с тех пор, как человек впервые научился выплавлять железо. Медь — мягкий металл, олово еще мягче. В незапамятные времена, когда еще не знали железа, случай натолкнул человека на твердый сплав меди и олова: бронзовый век предшествовал веку железному. И еще раньше — век каменный, век алюмосиликатов, когда человек совсем не знал простых тел — элементов.
Мысли Деви делают скачок через десятки веков.
…Эпоха расцвета химии — Лавуазье, Пристлей, Кавендиш, Шееле и другие открывают новые элементы. Становится известным все большее количество простых тел, из которых построена вся вселенная.
Кислород открыт в 1772 году Шееле, но в истории можно найти указание на более ранее знакомство с этим газом. Еще в XIII веке китаец Мао-Хоа упоминает о неизвестном газе; Леонардо да Винчи в XV веке знал две составные части воздуха, одна из которых участвовала в горении. Пристлей, независимо от Шееле, в 1774 году также открывает кислород. Лавуазье установил элементарную природу газа, дающего жизнь, и доказал, что вода — сложное вещество; он же установил неразложимость серы. Еще одним химическим элементом больше, одним научным заблуждением меньше.
Азот открыт Ретзефордом в 1772 году, Лавуазье дает новому газу название — азот (безжизненный). Еще три-четыре элемента, и обзор простых тел закончен. Неужели это все?
1807 год. Близится время, когда будут открыты новые простые тела, новые пути для победоносного движения химии.
В арсенале химика-исследователя едкие щелочи — едкие натр и кали занимают видное место с давних времен; они хорошо известны не только химикам, но и мыловарам и аптекарям. Едкие щелочи растворяют многие твердые тела; соединяясь с кислотами, они образуют соли. Общим признанием пользовалось утверждение, что щелочи есть простые тела, элементарные вещества. Они такие же элементы, как и железо, фосфор, сера.
Только Лавуазье в 1789 году посмел высказать сомнение в элементарности едких кали и натра. Он полагал, что щелочи есть окислы неизвестных металлов. Деви решил проверить это предположение.
Еще в 1800 году, производя первые химические опыты с применением Вольтова столба, Деви пытался разложить поташ химически, но ему удалось добиться только сгущения раствора у одного из полюсов батареи. В 1807 году Деви возвратился к той же задаче.
Небольшой Вольтов столб возвышается среди кажущегося беспорядка, столь привычного и необходимого страстной натуре молодого ученого. Но несмотря на свой темперамент, Деви неумолимо строг в документации научной работы. Ни один факт, ни одна цифра не должны миновать «Большой журнал», в научных экспериментах не следует доверяться памяти; сам Деви или его помощники под диктовку заносят в журнал данные всех исследований.
Записи указывали на самое главное. Точность соблюдалась только в мерах и весе, здесь — святая святых каждого сотрудника лаборатории. Деви никогда не окружал таинственностью свои работы, как это практиковали другие ученые: каждый мог познакомиться с журнальными записями. Более того, Деви не опасался принимать своих коллег непосредственно в лабораторной обстановке и рассказывать им о ходе своих исследований.
Так было и в 1807 году.
Первоначально Деви решил пропустить электрический ток через водный раствор едкого кали. Водный раствор кали при обычной комнатной температуре был подвергнут действию утроенной батареи: первая из 24 пар пластинок цинка и меди в 12 квадратных дюймов, вторая из 100 пар в 6 квадратных дюймов и третья из 150 пар пластинок в 4 квадратных дюйма, заряженных растворами квасцов и азотной кислоты. Это была тогда одна из наиболее сильных батарей в мире.
Реакция происходила бурно. Из горячего раствора вырывались пузырьки газов; это были кислород и водород. Но кислород и водород были уже открыты, и ничего нового электролиз водного раствора едкого кали не принес.
Брат Деви описывает состояние, в котором находился тогда Гемфри: «Я никогда не забуду его вида, Когда он бывал сильно погружен в свое любимое занятие. Его рвение доходило до энтузиазма, который сообщался всем окружающим. С радостным лицом и веселым голосом, руками, столь же быстрыми как и его ум, он был неутомим в своей работе. Успех его радовал, но неудачи он сносил с большим терпением. Вообще всякие неудачи и несчастные случаи во время экспериментов, даже происшедшие по вине учеников и помощников, он сносил с большим спокойствием, чем можно было бы ожидать от человека его темперамента».
На этот раз ученики и помощники ни в чем не были повинны. Дело застопорилось всерьез, и нужно было искать новые методы, чтобы заставить едкое кали открыть свою тайну. Деви не унывал. Энергия и напористость химика превышали возникавшие затруднения. План действий был изменен.
В платиновую ложечку, наполненную сухим едким кали, была направлена струя пламени спиртовой горелки. Чтобы температура была выше, в пламя вдувался кислород. Вскоре щелочь расплавилась; тогда привели в действие Вольтов столб. У проволоки, что сверху погрузилась в оранжево-красную массу щелочи, появился сильный зеленоватый свет и колонна пламени. Какое-то вещество сгорало над точкой соприкосновения проволоки со щелочью. Цвет пламени показал Деви, что это какое-то новое вещество, но как ни старался экспериментатор собрать это вещество, оно попрежнему оставалось неуловимым. Деви пишет об этих опытах: «Я произвел несколько опытов над электризацией кали, расплавленного нагреванием, в надежде собрать горючее вещество, однако безуспешно; мне удалось добиться желанного результата только тогда, когда я воспользовался электричеством в качестве общего начала для плавления и разложения».
Так как высушенная щелочь не проводит электричества, при новом варианте опыта у Деви возникло затруднение. Было решено отбросить спиртовку и не расплавлять в ее пламени сухую щелочь. Деви приступил к третьему опыту.
В этот октябрьский осенний день, как и обычно, Деви явился в лабораторию к 10 часам утра. Он взял платиновый кружочек и положил на него кусочек едкого кали. Необходимо несколько минут подержать щелочь на воздухе, чтобы она немного отсырела. Деви налаживал батарею; мерно стучал маятник больших старинных часов. Деви метался от одного места лаборатории к другому. Загремела стеклянная банка, осколки стекла рассыпались по полу. Желтый лондонский туман превратил день в ночь, сквозь пелену тумана тускло светили газовые рожки уличных фонарей… По Альбемарл-стрит, словно призраки, плыли мрачные тени прохожих. Прошли секунды, наступило время действовать.
В своей Bakerian Lecture — Бакеровской ежегодной лекции[17], читанной 20 ноября 1807 года, Деви рассказывает об этом решающем опыте:
«Маленький кусочек кали, который в течение нескольких секунд был выставлен на воздух, так что его поверхность сделалась проводящей, был помещен на изолированный платиновый диск, соединенный с отрицательным полюсом интенсивно действовавшей батареи в 250 пластин с поверхностью в 6 дюймов и в 4 дюйма; в то же время платиновая проволока, соединенная с положительным полюсом, была приведена в соприкосновение с верхней поверхностью щелочи. Весь прибор находился на открытом воздухе.
При этих условиях вскоре обнаружилось энергичное действие. Кали начал плавиться у обеих точек электризации, причем у верхней поверхности наблюдалось энергичное выделение газа, у нижней — отрицательной поверхности — газ не выделялся. Вместо этого появлялись маленькие шарики с сильным металлическим блеском, внешне ничем не отличавшиеся от ртути. Некоторые из них сейчас же после своего образования сгорали со взрывом и с появлением яркого пламени, другие не сгорали, а только тускнела, и поверхность их покрывалась в конце концов белой пленкой.
Многочисленные опыты вскоре показали, что эти шарики состоят из того вещества, которое я искал и которое является легко воспламеняющимся основанием кали».
Когда Деви увидел крохотные крупинки нового вещества, загоревшиеся в воздухе, он запрыгал, как ребенок, по комнате, не будучи в силах сдержать свою радость.
Лихорадочная работа продолжалась. Изучались свойства открытого элемента, готовился опыт для разложения другой едкой щелочи — едкого натра. Для разложения натриевой щелочи понадобился Вольтов столб большей мощности. Если для разложения 40–70 граммов едкого кали было достаточно 100 шестидюймовых пластин, то для разложения едкого натра пришлось применить батарею в 250 пластин. Шарики нового вещества, полученного уже не из едкого кали, а из едкого натра, напоминали своего сородича. В момент своего образования они часто сгорали, иногда же распадались на меньшие шарики и с большой скоростью проносились по воздуху. Они напоминали маленький фейерверк, образуя удивительно красивые огненные струи.
Открытые элементы обладали рядом чудесных свойств. Эти металлы не терпели одиночества. Один из них на воздухе быстро покрывался пленкой, а, окисляясь, вскоре превращался в жижу едкого кали, то есть возвращался в исходное состояние. Деви жалуется на трудность сохранения нового вещества. В соляной кислоте оно самовозгорается ярким красным светом. Брошенное в воду или приведенное в соприкосновение с каплей воды, оно мгновенно взрывается и, разбрасывая искры, бегает по поверхности воды; в результате снова получается раствор едкого кали. Если такой шарик поместить на лед, он сейчас же загорается ярким пламенем, причем во льду образуется углубление, содержащее раствор едкого кали. Новое вещество, нагретое в смеси с окислами металлов, легко их восстанавливает. Таким образом, из окиси цинка или свинца можно получить сплав этих металлов с их новым собратом, И только в керосине резвый металл вел себя спокойно, там он как бы умиротворялся.
Деви изучил основные свойства металла, полученного из едкого кали. Самым замечательным из них являлся малый удельный вес: металл был легче воды. Он отличался неуемной страстью к кислороду: где бы ни был кислород, это вещество настигало его и бурно соединялось с ним.
Свойства металла из едкого натра, как упоминалось, были схожи со свойствами металла из едкого кали, это были близнецы. Только натровый металл был немного спокойней калиевого. Он также был легче воды, также окислялся на воздухе, покрываясь пленкой едкого натра, правда, значительно медленнее, чем тот, что из кали. В кислороде новое вещество горело белым пламенем, разбрасывая яркие, очень красивые искры. Брошенный в воду, он не горел, но, шипя, с бурным выделением газа, подпрыгивая, бегал по поверхности воды.
Деви подводит итог своим замечательным открытиям: «Можно ли назвать основания кали и натра металлами? Большинство ученых, которым был поставлен этот вопрос, отвечали на него утвердительно. Действительно, тела эти сходятся с металлами по блеску, ковкости, по способности проводить тепло и электричество и по своим химическим свойствам.
Вряд ли можно считать их низкий удельный вес достаточной причиной для того, чтобы выделить их в новую группу тел, ибо и между металлами в этом отношении наблюдаются заметные колебания: так, платина в четыре раза тяжелее теллура. Кроме того, при установлении научного разделения тел на группы нужно руководствоваться аналогиями между возможно большим количеством свойств.
Поэтому я полагаю, что при построении названий для этих металлов нужно воспользоваться теми же окончаниями, что и для других новооткрытых металлов. Окончания эти, по своему происхождению являются латинскими, но теперь они у нас общеупотребительны.
«Калий» и «Натрий» (т. е. Potassium и Sodium) — вот имена, которые я решился дать двум новым веществам, и какие бы изменения ни произошли впоследствии в теориях, касающихся строения тел, вряд ли в этих терминах может содержаться ошибка; их можно рассматривать просто как обозначения для металлов из кали и натра. По поводу этого словообразования я советовался со многими выдающимися учеными нашей страны, и большинство одобрило мой выбор.
Возможно, что названия эти более выразительны, чем изящны, но я не мог найти других названий, говорящих о каком-нибудь специфическом свойстве, которое не было бы общим у обоих элементов. Для основания натра можно было бы еще почерпнуть что-нибудь в греческом языке, но аналогичный метод нельзя применить к основанию кали, ибо древние, повидимому, не знали различия между двумя видами щелочей».
С нечеловеческой энергией все дальше продвигался Деви в глубь неизведанных проблем. Он уже пробовал разлагать барит, предвидя в нем еще неоткрытый элемент — барий; он разлагал стронциан в поисках еще неизвестного элемента — стронция. Все дальше шел молодой и смелый ученый. Он уже мечтал о разложении извести, в которой искал кальций, он мысленно разлагал магнезию — здесь он пророчески предвидел магний, и, наконец, он пробовал при помощи Вольтова столба разложить окись алюминия (глинозем).
На этом стоит остановиться подробней. В его записках читаем: «Если бы мне посчастливилось получить металлическое вещество, которое я ищу, я предложил бы для него название — алюминий».
Задача получить из глинозема алюминий была поставлена в науке впервые. Деви был настолько убежден в своей победе, что заранее дал название новому металлу.
…Деви дописывал текст лекции; завтра, с высоты кафедры Королевского общества, он поведает миру о своем открытии. «Широкое поле для исследований открывается, благодаря активности и сродству новых металлов, выделенных из щелочей.
Металлы эти, несомненно, станут могущественными средствами анализа, и, обладая сродством к кислороду, которое превышает сродство всех других известных веществ, они, возможно, окажутся более эффективными, чем электричество по отношению к некоторым из еще неразложенных тел. Так, я нашел, что основание кали окисляется в углекислоте, разлагая ее; будучи нагрето с углекислой известью, оно выделяет углерод. Подобным же образом оно окисляется и в соляной кислоте (я не имел случал произвести этот опыт настолько точно, чтобы выяснить, что происходит).
Знакомство с природой щелочей и выводы, к которым, по аналогии, оно приводит, открывают ряд новых горизонтов. Быть может, оно позволит решить многие геологические проблемы и покажет, что в образовании горных пород принимали участие силы, о существовании которых до сих пор и не подозревали.
Легко было бы еще более распространить эти гипотетические соображения, но я не хочу далее отнимать время у общества, тем более, что целью моей лекции было не построение гипотез, а изложение ряда новых фактов».
Более 800 000 книг и аудиокниг! 📚
Получи 2 месяца Литрес Подписки в подарок и наслаждайся неограниченным чтением
ПОЛУЧИТЬ ПОДАРОКЧитайте также
Великие умы
Великие умы В принстонской аспирантуре я работал под руководством Джона Уилера. Он поставил передо мной задачу, но она оказалась слишком трудной, и никаких результатов я не получил. Поэтому я обратился к идее, которая возникла у меня раньше, еще в МТИ. Состояла эта идея в
Эксперименты и открытия
Эксперименты и открытия Наш путь лежит в знаменитый Академгородок, который находится в Новосибирской области. Мы договорились о встрече с известным ученым, доктором биологических наук Дмитрием Владимировичем Терновским. Он уже более 40 лет изучает семейство
ГЛАВА ВОСЬМАЯ Первые годы работы профессором в университете Джона Гопкинса. Важные открытия. Прометеевское празднование открытия
ГЛАВА ВОСЬМАЯ Первые годы работы профессором в университете Джона Гопкинса. Важные открытия. Прометеевское празднование открытия После смерти знаменитого и грубоватого Генри Роуланда в университете Дж. Гопкинса в 1901 году Вуду была предложена должность «полного»
ПРОЦЕСС ОТКРЫТИЯ
ПРОЦЕСС ОТКРЫТИЯ Чаще всего после вопроса «Почему вы делаете ту работу, которую делаете?» мне задают следующий вопрос: «Как вы определяете активность нового препарата?»Как можно судить о воздействии и природе этого воздействия, которое оказывает на центральную нервную
ПЕРВЫЕ ОТКРЫТИЯ
ПЕРВЫЕ ОТКРЫТИЯ Мои первые творческие открытия не имели ничего общего ни с наукой, ни с искусством. Они были бытовыми. В Москву меня отправили в ботинках. Но ботинки были женские. Чтобы меня не дразнили за это, я догадался заворачивать верх ботинок внутрь так, что
Важные открытия
Важные открытия Наверное, покажется странным, но что поделаешь, так уж случилось, что до поступления в театральное училище имени Б. В. Щукина я ни разу не был в Вахтанговском театре, не знал даже ведущих его актеров — М. Ф. Астангова, Н. О. Гриценко, Н. С. Плотникова,
Великие открытия Пастера
Великие открытия Пастера Пастер не сразу принялся за изучение болезнетворных микробов. Химик по образованию, он первоначально проделал огромную работу по выяснению причин брожения и гниения. В том и в другом случае к этому были причастны микроорганизмы. Пастер
День открытия
День открытия 31 мая 2013, 20:43 вечераЭтот день никогда не забуду. И не потому, что открытие…День самый сумасшедший из всех последних. Не хочу описывать в подробностях, но сегодня очень много разных событий произошло, а могло и не произойти, масса факторов, которые могли не
ОТКРЫТИЕ ОТКРЫТИЯ
ОТКРЫТИЕ ОТКРЫТИЯ Но разве тогдашняя Россия была сплошной безлюдной пустыней для науки? Да нет, конечно! Русскую науку и тогда двигали вперед могучие умы великих ученых, снискавших мировое признание. И они, со своей стороны, стремились, как могли, поддержать удивительного
Открытия
Открытия Мы вернулись на Малиновскую, восвояси.Я опять окунулся в уютную и родную среду, что была мне знакома с младенчества — с той поры, когда меня привозили в Харьков показывать бабушке, крестить в церкви, знакомить с дядьями, братьями, домом, округой…И хотя я не застал
Ни года без открытия
Ни года без открытия По возвращении в Россию Дмитрий Иванович продолжил теоретические и практические исследования в различных областях физики, химии и других наук. Значительными открытиями и научными достижениями был отмечен едва ли не каждый год его долгой карьеры. В
Поздние открытия
Поздние открытия Поражает, до какой степени непредсказуемо высок накал человеческих страстей, когда сближаются два «электрода» — мужчина и женщина. И молниеносно подключается всё, вся система, весь генезис, уводящий в века и одновременно ткущий стратегию новых